HIV-Impfung: Zeit für eine neue Taktik
Bereits 1983 entdeckten die Virolog:innen Françoise Barré-Sinoussi und Luc Montagnier das Humane Immundefizienz-Virus Typ 1 (HIV-1). Heute – 40 Jahre später – ringen Forschende immer noch damit, Strategien gegen den Erreger der Immunschwächekrankheit AIDS zu entwickeln. „Viren sind Meister des Verwandelns. Das gilt besonders für HIV, weil das Virus eine hohe Mutationsrate hat und unserem Immunsystem stets einen Schritt voraus ist“, sagt Doris Wilflingseder, Professorin für Infektionsbiologie an der Medizinischen Universität Innsbruck.
Wilflingseder erforscht, wie das menschliche Immunsystem auf Krankheitserreger reagiert. In einem vom Wissenschaftsfonds FWF geförderten Projekt charakterisierte ihr Team, welche Signalwege eine Neuinfektion mit HIV auslöst. Die Forschenden entdeckten, dass die Viruspartikel von bestimmten Eiweißen umhüllt werden, die für ihre weitere Verarbeitung entscheidend sind. Nun möchten sie das gewonnene Wissen für einen Impfstoff nutzen, der ebendiese Signale imitiert, um eine besonders starke Immunantwort auszulösen.
Hunderte Neuinfektionen pro Jahr
Die Österreichische AIDS-Gesellschaft schätzt, dass hierzulande 9.000 Menschen mit einer HIV-Infektion leben. Pro Jahr werden ca. 400 Neuinfektionen festgestellt, wobei man davon ausgehen kann, dass jede zehnte infizierte Person noch nicht getestet wurde und über ihre Infektion nicht Bescheid weiß.
HIV wird über das Blut, über Sperma, Vaginalsekret und andere infektiöse Körperflüssigkeiten übertragen. Wenn die Viruspartikel in den Organismus eindringen, treffen sie wie alle Krankheitserreger auf eine erste Schutzbarriere (unspezifische Immunabwehr). Diese unterdrückt den Infekt in den ersten zwei bis drei Wochen, bis die spezifische Immunantwort einsetzt, die HIV-spezifische Immunzellen (T-Zellen) und Antikörper umfasst. Wilflingseder fand heraus, dass die Viruspartikel in der Akutphase von einem Mantel aus Proteinen umhüllt werden. „Im Gegensatz zu ‚nackten‘ Viruspartikeln löst HIV ummantelt mit Akutphase-Proteinen eine stärkere Immunantwort aus“, fasst sie die Ergebnisse zusammen.
Zur Person
Doris Wilflingseder erforscht am Institut für Hygiene und Medizinische Mikrobiologie der Medizinischen Universität Innsbruck die Interaktionen zwischen Krankheitserregern und ihren Wirten. Im Rahmen ihrer wissenschaftlichen Arbeit engagiert sich die Professorin für Infektionsbiologie auch für eine Forschung ohne Tierversuche, unter anderem durch die Gründung des MUI animalFree Research Cluster. Das Projekt „HIV-C entflieht Restriktion, nicht Sensing in DCs“ läuft bis Mai 2024 und wird vom Wissenschaftsfonds FWF mit knapp 407.000 Euro gefördert.
Neue Strategie für einen Impfstoff
Die Forschungsergebnisse zeigen, dass unser Immunsystem in der Akutphase eine HIV-Infektion am stärksten erwidert. Der Effekt wird abgeschwächt, wenn im weiteren Verlauf spezifische, nicht hemmende Antikörper auf der Erregeroberfläche binden. „Das ist wichtig, denn eine chronische Aktivierung der Immunreaktion könnte zu Organschäden führen“, erklärt Wilflingseder.
Um einen neuen Weg in der Impfstoffentwicklung einzuschlagen, will ihr Team die Reaktionen der Akutphase nachstellen. „Dafür haben wir die Signalwege und Mechanismen der unspezifischen Immunantwort im Detail erforscht“, sagt Wilflingseder. „In Zusammenarbeit mit lokalen, nationalen und internationalen Expert:innen zielen wir auf einen Impfstoff ab, der dieselben Rezeptoren anspricht wie solch umhülltes HIV.“ So soll der Impfstoff den effektiveren Signalweg in Gang setzen, was die Fähigkeit von Immunzellen verbessert, fremde Molekülstrukturen aufzunehmen und eine Immunantwort in den regionalen Lymphknoten zu induzieren.
Das Komplementsystem
Der Mechanismus, den sich die Forschenden zunutze machen, basiert auf einem bekannten, aber bei HIV bislang vernachlässigten Teil der unspezifischen Immunabwehr: dem Komplementsystem. Damit wird eine Gruppe von löslichen Proteinen bezeichnet, die von diversen Krankheitserregern aktiviert werden und bestenfalls deren Zerstörung initiieren beziehungsweise den Krankheitserreger in Schach halten, bis die spezifische Immunantwort greift.
Die Proteine des Komplementsystems liegen unter anderem im Blut und in der Samenflüssigkeit vor und bilden um das HIV-Partikel einen Mantel. Trifft ein solches von Komplementfaktoren umhülltes Virus auf eine Immunzelle, dann wird es von anderen Rezeptoren als nacktes HIV erkannt. „In der Forschung untersuchte man eher die Wechselwirkungen des ‚nackten‘ Virus mit isolierten Zelltypen. Doch der Erreger liegt im Körper nicht in dieser Form vor. Deshalb stellen wir in unseren Experimenten den Beginn einer Infektion so realistisch wie möglich mittels Zellkulturen nach“, erklärt Wilflingseder.
Was passiert bei der Infektion?
Sowohl bei der HIV-Infektion als auch bei einer potenziellen Impfung sind es die dendritischen Zellen, die als erste Immunzellen auf den Partikel treffen. „Sie liegen im Gewebe vor und reagieren als ‚Wächterzellen‘ des Immunsystems sofort, wenn ein Krankheitserreger in den Organismus gelangt“, erklärt Wilflingseder. Erstens schütten sie antivirale lösliche Stoffe (Interferone) aus, die den Infekt zügeln. Zweitens „fressen“ und zerkleinern die dendritischen Zellen das Virus und wandern in den nächstgelegenen Lymphknoten, wo sie die spezifische Immunabwehr lostreten.
„Wenn ein HIV-Partikel einen Komplement-Mantel trägt, dann wird es von den dendritischen Zellen vollkommen anders aufgenommen und prozessiert“, so Wilflingseder. Nackte HIV-Partikel werden ebenso wie die späteren antikörperumhüllten Viren in der dendritischen Zelle unterdrückt. Deshalb lösen sie eine nur mäßige Immunantwort aus. Im Gegensatz dazu gelangt von Komplementfaktoren umhülltes HIV bis in den Zellkern und infiziert die dendritischen Zellen. Das wiederum bewirkt eine starke Immunantwort, die die Viruslast in der Akutphase senken kann.
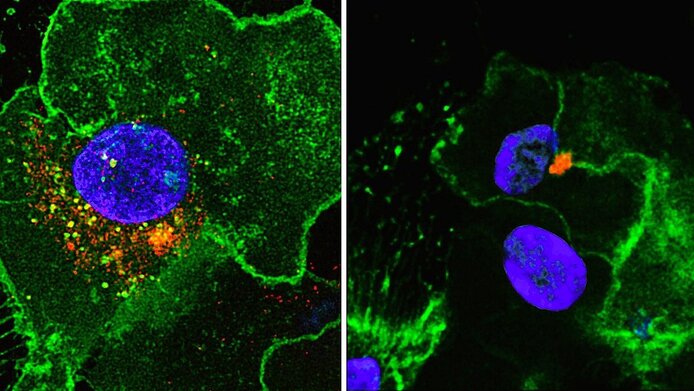
„Dass es zur Infektion der dendritischen Zellen kommt, ist ein zweischneidiges Schwert“, räumt Wilflingseder ein. „Aber wir konnten zeigen, dass eine minimale produktive Infektion der Zellen dazu beiträgt, dass das Virus vom Körper besser wahrgenommen wird.“ Denselben Effekt bewirkt der weniger verbreitete Subtyp HIV-2, der eine AIDS-Erkrankung nachweislich langsamer auslöst als HIV-1.
Umdenken gefragt
„Üblicherweise wird bei Impfungen vermieden, das Komplementsystem zu aktivieren, damit es zu keinen übermäßigen Immunreaktionen kommt. Unsere Forschungsergebnisse weisen aber darauf hin, dass wir bei der HIV-Impfstoffentwicklung umdenken müssen“, bekräftigt Wilflingseder.
Bleibt die Frage, ob die HIV-Impfung damit nach 40 Jahren Forschung in greifbare Nähe rückt? „Ein Paradigmenwechsel hin zu einer Komplementaktivierung muss natürlich akkurat untersucht werden. Er kann nur dann erreicht werden, wenn die in der Zellkultur beschriebenen positiven Effekte im Organismus genauso hervorgerufen und überschießende Immuneffekte vermieden werden – insofern ist es schwierig, hier eine zeitliche Prognose abzugeben“, so die Antwort der Expertin. Dennoch zeigen die Ergebnisse, dass sich auch in einem breit erforschten Gebiet noch ungeahnte Wege auftun können.





