Menschlicher Botenstoff in Live-Show
Seit der Entdeckung seiner Rolle für die erektile Dysfunktion ging es aufwärts – mit der Bekanntheit von Stickstoffmonoxid (NO) als Regulator wichtiger Funktionen des Herz-Kreislauf-, Nerven- und Immunsystems. Direkte Echtzeitmessungen seiner zellulären Konzentration waren bis jetzt aber nicht möglich. Mit Unterstützung des Wissenschaftsfonds FWF gelang das nun einer Gruppe um Roland Malli am Institut für Molekularbiologie und Biochemie der Medizinischen Universität Graz.
Leuchtprotein
Das Team stellte ein leuchtendes Protein her, dessen Fluoreszenz sich bei Bindung von NO verändert. Dabei ist diese Änderung der Fluoreszenz von der Konzentration des NOs abhängig, reversibel und erfolgt quasi in Echtzeit –, also alles, was benötigt wird, um intrazelluläre Messungen der NO-Dynamik vornehmen zu können. Die Messung solcher Dynamiken gelang Malli in der Folge in verschiedenen Zelltypen. Diese wurden genetisch so modifiziert, dass sie das neue Protein selbst herstellten und die NO-Konzentration einfach anhand der emittierten Fluoreszenz gemessen werden konnte.
Die Chimäre
Wesentlich für die Arbeit der Gruppe waren dabei Proteine, die NO mit hoher Spezifität binden. "Wir überlegten uns", erläutert Malli, "ein solches NO-Bindungsprotein mit einem natürlich fluoreszierenden Protein zu verbinden. Quasi ein chimäres, neues Protein zu schaffen, das sowohl NO binden als auch fluoreszieren könnte." Die Annahme war, dass die Fluoreszenz des neuen Proteins sich dann ändern würde, wenn es NO bindet. Computersimulationen bestätigten dies für ganz spezielle Kombinationen von Proteinen.
Basteln mit Proteinen
Der Simulation folgend begann Malli, eine Anzahl neuer Proteine herzustellen. Bei all diesen stammte der NO-Bindungsteil von einem als NorR bezeichneten bakteriellen Protein. Dies ist ein sogenannter Transkriptionsfaktor, der als Vermittler zwischen einem NO-Signal und der Aktivierung von genetisch gespeicherter Information dient. Zum Vorteil der Verwendung eines bakteriellen Proteins meint Malli: "Die Wahrscheinlichkeit war hoch, dass dies selbst wenig Einfluss auf Säugetierzellen nehmen würde, in denen NO gemessen werden sollte." In der Folge fusionierte das Team jenen Teil von NorR, der speziell für die NO-Bindung verantwortlich ist, mit fünf verschiedenen fluoreszierenden Proteinen. Tatsächlich wurden die als "genetically encoded NO probes" (geNOps) bezeichneten Fusionsproteine dabei so hergestellt, dass ihre genetische Information, in Zellen eingebracht, rasch zur Biosynthese funktionstüchtiger NO-Sensoren führte.
Weniger ist mehr
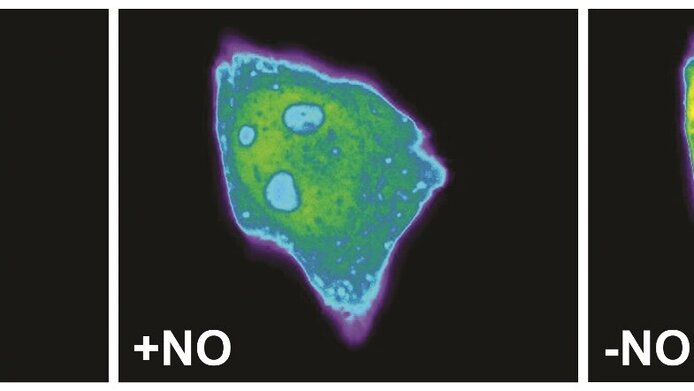
Über die hohe Wirksamkeit der verschiedenen geNOps war Malli dann selbst überrascht: "Die Bindung des NOs führte, wie erwartet, zu einer Reduktion – einem sogenannten Quenching – der Fluoreszenz“, berichtet Malli. „Der Effekt ist dabei ganz eindeutig zu messen und ist in seiner Intensität direkt von der NO-Konzentration abhängig. Dazu kommt, dass die NO-Bindung leicht reversibel ist, was erlaubt, sehr schnelle Änderungen der zellulären NO-Konzentration zu messen. Es ist wirklich ein fantastischer Fortschritt!"
Patente Technik
In der Folge konnte das Team um Malli dann sogar die NO-Konzentration in zellulären Kompartimenten, wie den Mitochondrien, messen. Zusätzlich kombinierten sie den Einsatz von geNOps mit der Messung der Kalzium-Konzentration in Zellen und konnten so mit hoher zeitlicher Auflösung Zusammenhänge in der Aktivität der Botenstoffe NO und Kalzium zeigen. Die mit Unterstützung des FWF erfolgte Entwicklung der bereits patentierten geNOps eröffnet eine neue Ära der Messung von Stickstoffmonoxid und seiner vielfältigen physiologischen Wirkungen auf der Ebene einzelner Zellen.
Zur Person Roland Malli ist am Institut für Molekularbiologie und Biochemie der Medizinischen Universität Graz tätig und befasst sich insbesondere mit der Messung intrazellulärer Ionen und ihrer Rolle als Signalstoffe. Neben elektrophysiologischen Ansätzen entwickelt er dazu insbesondere mikroskopische Verfahren weiter und wurde im vergangenen Jahr mehrfach für seine patentierten Entwicklungen ausgezeichnet.
Originalpublikation





