Bewährte Biochemie für neue Hautkrebstherapie

Patientinnen und Patienten mit Herz-Kreislauf-Beschwerden bekommen seit vielen Jahren Ernährungsempfehlungen, um die Cholesterinwerte im Blut zu verbessern. Diese basieren letztlich auf Erkenntnissen zur Rolle der Blutfette im Stoffwechsel: Die Cholesterinaufnahme, -abgabe und -verteilung ist gut untersucht, ebenso wie die Rolle von Cholesterin in Signalketten und im Membranaufbau von Zellen. In einem kürzlich abgeschlossenen FWF-Projekt konnten Clemens Röhrl und sein Team am Zentrum für Pathobiochemie und Genetik der Medizinischen Universität Wien zeigen, dass gerade aus der Vernetzung bereits bekannter biochemischer Prozesse, Methoden und Daten ganz neue Erkenntnisse für die Identifikation und Behandlung von Krebs gewonnen werden können. Unterstützt vom Wissenschaftsfonds hat der Biochemiker auffällige Prozesse im Cholesterinstoffwechsel gutartiger und bösartiger Hautkrebszellen untersucht.
Fatale Wanderlust
Das bösartige Melanom ist ein seltener Tumortyp, dafür aber sehr aggressiv. Wenn der schwarze Hautkrebs spät erkannt wird, hat er oft schon gestreut und die Betroffenen deswegen eine geringe Überlebenswahrscheinlichkeit. Bei ungefähr 30 Prozent der Behandelten schlagen Immuntherapien gegen Hautkrebs gut an. Umgekehrt bedeutet das: Rund 70 Prozent der Behandelten bekommen eine Therapie, die bei ihnen nicht hilft, Nebenwirkungen hat und teuer ist. „Es gibt aktuell keine Möglichkeit den Erfolg vorherzusagen. Speziell beim Melanom kommt man mit einer einzigen spezifisch wirkenden Medikation allein nicht weiter, es braucht den gleichzeitigen Angriff auf mehrere Schwachstellen“, beschreibt Clemens Röhrl die Ausgangssituation. Als Biochemiker hat er sich auf den zellulären Fettstoffwechsel spezialisiert und weiß daher, dass alle Zellen im Körper Cholesterin brauchen, gutartige und bösartige. Für sein Einzelprojekt zog er Expertise innerhalb der Medizinischen Universität Wien zusammen. Ein wichtiger Kooperationspartner in dem interdisziplinären Projekt war Krebsforscher Mario Mikula, ebenfalls vom Zentrum für Pathobiochemie und Genetik. Das Team untersuchte mit einem bewährten Methoden-Set Hautkrebszelllinien: solche, die Metastasen bilden und solche, die an Ort und Stelle wuchern.
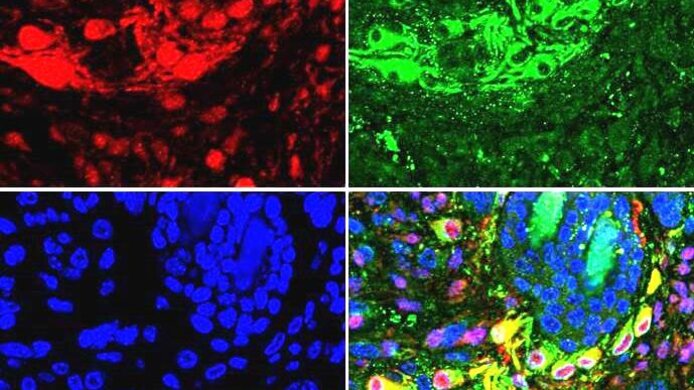
Cholesterinrezeptor auf Abwegen
In vitro wurde zunächst untersucht, welche Zelllinien eine starke Genaktivierung für die Bildung verschiedener Cholesterinrezeptoren aufweisen. Zudem wurde bestimmt, welche Rezeptoren vermehrt gebildet werden: „Es zeigte sich, dass die Genaktivität für den Rezeptor SR-B1, der in gesunden Zellen HDL-Cholesterin bindet und eine Schutzfunktion hat, in metastasierenden Hautkrebszellen besonders hoch ist“, erklärt Röhrl im Gespräch mit scilog. Ein erster Ansatzpunkt für einen Marker, der sich für die Vorhersage des Therapieerfolges eignen könnte. In einer nächsten Versuchsreihe wurde die Genexpression für diesen Rezeptortyp in gutartigen Zellkulturen gesteigert oder gedrosselt. So wurde festgestellt, dass bei einer verstärkten Genexpression für den SR-B1-Rezeptor auch in gutartigen Zelllinien eher Metastasen gebildet werden. Um diese experimentellen Ergebnisse zu prüfen, durchsuchte das Team mit bioinformatischen Methoden bestehende Datensätze aus der Hautkrebsforschung gezielt nach Cholesterin-Rezeptoraktivität und Überlebenswahrscheinlichkeit: „Auf diese Weise bekamen wir Zugang zu Humanstudien, für die niemand erneut mit Untersuchungen belastet wurde. In den Datensätzen fanden wir ebenfalls eine Korrelation zwischen der starken SR-B1-Genexpression und einer schlechten Überlebensprognose bei Hautkrebs-Patientinnen und Patienten.“ Ein weiterer Ansatzpunkt zur Charakterisierung von gefährlich wanderfreudigen Hautkrebszellen ist die „ER-Stress-Response“. Dieses biochemische Signal wird von der zentralen Proteinsynthese und Proteintransport-Einheit der Zelle ausgelöst, wenn es ein Ungleichgewicht in der Proteinproduktion gibt. In weiterer Folge fahren gesunde Zellen Anpassungsmechanismen oder lösen den programmierten Zelltod aus. Auch hier verhalten sich metastasierende Melanome ungewöhnlich: Sie zeigen ein starkes Stresssignal, sterben aber nicht ab. Stattdessen schütten sie Wachstumsfaktoren aus und machen sich bereit auszuwandern, also Tumorzellen zu streuen. Der Einsatz eines zugelassenen Medikaments, das den ER-Stresslevel drosselt, aber bisher zur Behandlung eines anderen Krankheitsbildes eingesetzt wurde, war in den isolierten Zelllinien zwar erfolgreich, schlug im Tiermodell aber fehl. Im Mausmodell konnte die Metastasierung so nicht zurückgedrängt werden. Mit Standardmethoden der Stoffwechsel-Biochemie in der Krebsforschung ist dennoch ein erster Brückenschlag gelungen, der begleitenden Therapieansätzen oder Abkürzungen bei der Zulassung von Wirkstoffen den Weg ebnen könnte.
Zur Person Clemens Röhrl forscht an der Medizinischen Universität Wien zu Physiologie und Pathophysiologie des Fettstoffwechsels. Er hat Ernährungswissenschaften und Lebensmittelchemie studiert und am Department of Cancer Research der Medizinischen Universität Wien seine Diplomarbeit absolviert, arbeitete als Postdoc am Department für Medizinische Chemie und hat sich im Jänner 2018 in medizinischer Biochemie habilitiert.
Publikationen





