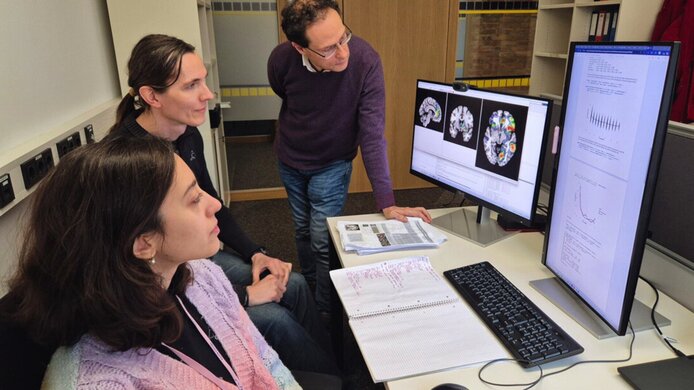
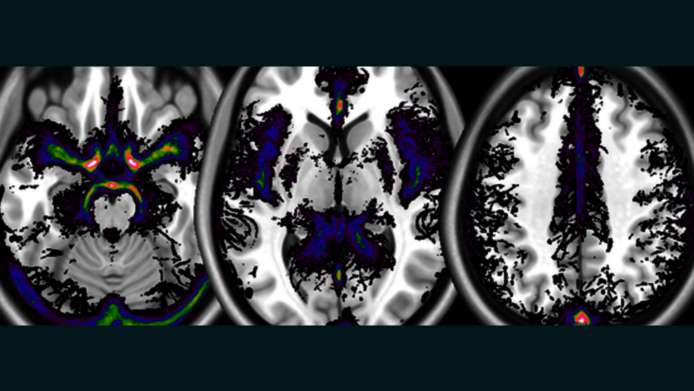
„Die Ergebnisse deuten darauf hin, dass wir neben dem Cortex auch andere wichtige Signale haben, die nicht von Neuronen stammen“, erklärt Viviani. Er vermutet dahinter einen Mechanismus des unwillkürlichen Nervensystems, der gleichzeitig auf die Durchblutung des Gehirns und des Schädelknochens wirkt. Wie sich diese Unterschiede auf die Verarbeitung emotionaler Reize auswirken, die auch in der Depression anders wahrgenommen werden, soll in weiteren Studien untersucht werden. Im nächsten Schritt will das Team Aufnahmen von Personen analysieren, die aktiv Aufgaben lösen oder Reize wahrnehmen, anstatt wie bisher in Ruhelage zu sein.
Nur mit internationaler Zusammenarbeit möglich
Darüber hinaus beteiligt sich Viviani im Rahmen der Kooperation an Studien zum individuell unterschiedlichen Ansprechen auf Psychopharmaka, insbesondere Antidepressiva. „Gemeinsam mit Partnern aus Deutschland haben wir statistische Modelle entwickelt, um den Einfluss von genetischen Varianten in wichtigen Enzymen auf den Medikamentenstoffwechsel zu beschreiben“, berichtet Viviani.
Die internationale Zusammenarbeit sieht er als entscheidend an, um solche umfassenden Datenplattformen zusammenstellen zu können. „Wir brauchen die Daten aus der Gesundheitsversorgung, vor allem in der Ära der KI“, ist Viviani überzeugt, auch wenn nationale Datenschutzvorgaben den Austausch von sensiblen Informationen teilweise stark einschränken. Eine datenbasierte personalisierte Medizin, wie sie durch ERA PerMed vorangetrieben werden soll, könnte Menschen mit Depression präzisere Diagnosen und individuell angepasste Therapien bieten – und das europaweit.